メタンハイドレートからメタンを回収するメカニズムをスパコン「京」で解明
2014年03月14日
岡山大学大学院自然科学研究科(理学部)理論化学研究室の矢ヶ崎琢磨特任助教、松本正和准教授、田中秀樹教授および名古屋大学工学研究科の研究チームは、独立行政法人理化学研究所計算科学研究機構のスーパーコンピュータ「京」を用いたシミュレーションにより、メタンハイドレートが分解しメタンが分離するメカニズムを世界で初めて解明しました。
本研究成果は2014年2月7日、アメリカ化学会の国際科学雑誌「Journal of Physical Chemistry B」オンライン版に掲載されました。
今回のメタンハイドレートの分解メカニズムの発見は、メタンガスの効率的な採取方法の研究に応用することができると期待されます。
<業 績>本研究成果は2014年2月7日、アメリカ化学会の国際科学雑誌「Journal of Physical Chemistry B」オンライン版に掲載されました。
今回のメタンハイドレートの分解メカニズムの発見は、メタンガスの効率的な採取方法の研究に応用することができると期待されます。
岡山大学大学院自然科学研究科(理学部)理論化学研究室の矢ヶ崎琢磨特任助教、松本正和准教授、田中秀樹教授および名古屋大学大学院工学研究科の研究チームは、独立行政法人理化学研究所計算科学研究機構のスーパーコンピュータ「京」を用いたシミュレーションにより、メタンハイドレートが分解しメタンが分離するメカニズムを世界で初めて解明しました。
この研究では岡山大学の研究グループが、さまざまな温度でのメタンハイドレート分解過程について、スパコン「京」を用いて10万分子以上の大規模シミュレーションを実施し、メタン分離の速度について新たなメカニズムを見出すことに成功しました。このシミュレーションには、名古屋大学の研究グループが「京」のために開発したソフトウェア「MODYLAS」が使われています。
今回の研究では、このメカニズムにおいて、ハイドレートが分解する過程でのメタンの過飽和水溶液と、それから生じる気泡が重要な役割を果たしていることを発見しました(図1)。これは今までの小規模な計算機では検証できない現象であり、計算速度が毎秒1京回を誇るスパコン「京」の利用により、世界で初めて検証できる現象となりました。
本研究により、気泡の生成を抑制したり、逆に促進したりすることで、メタンハイドレートの分解速度を制御できることが示唆されました。
<見込まれる成果>
メタンハイドレートは、水とメタンからできたシャーベット状の氷で、着火すれば分解してメタンが燃焼するために、「燃える氷」と呼ばれています。このメタンハイドレートは日本近海の大陸棚などに大量に存在し、エネルギー資源として大きく注目を集め、大規模な試掘も開始されています。メタンの燃焼によって生じる二酸化炭素はメタン自身よりも温室効果が小さく(1/20)、またメタンハイドレートは他の化石燃料の2倍以上の埋蔵量が期待されています。さらに、メタンハイドレートをメタンの貯蔵や輸送に使うことも考えられています。
メタンハイドレートの資源や貯蔵手段としての効率的な利用を図るために、その基礎科学の発展が待望されてきました。今回の研究は、実験と相補的関係にあり、実験だけでは困難な微視的な物性の正確な予測を通じて、メタンハイドレートの制御方法の指針を示しました。これは、ひいてはメタンガスの効率的な採取方法の研究の応用へとつながります。
<用語解説・参考文献>
1) メタンハイドレート
水と油は混ざらないものの代表例ですが、実際、メタンをはじめエタン、プロパンなどは液体状態の水に対する溶解度が非常に低く、分子数の比でいえば一万分の1以下しか溶けません。ところが、温度を下げると、メタンは水に対して15%以上もの割合で取り込まれてメタンハイドレート結晶になります。
メタンハイドレートの中では、水分子は通常の氷と同じように、水素結合で隣同士緊密につながりあいつつ、ゲスト分子を収容する空洞を形作っています(図2)。
通常の氷は、圧力をかけると融解しますが、メタンハイドレートでは逆にメタンガスの圧力を下げるとメタンハイドレートが分解しやすくなるので、温度を上げるほかに減圧をすることでも、メタンを取り出すことが出来ます。
水と油は混ざらないものの代表例ですが、実際、メタンをはじめエタン、プロパンなどは液体状態の水に対する溶解度が非常に低く、分子数の比でいえば一万分の1以下しか溶けません。ところが、温度を下げると、メタンは水に対して15%以上もの割合で取り込まれてメタンハイドレート結晶になります。
メタンハイドレートの中では、水分子は通常の氷と同じように、水素結合で隣同士緊密につながりあいつつ、ゲスト分子を収容する空洞を形作っています(図2)。
通常の氷は、圧力をかけると融解しますが、メタンハイドレートでは逆にメタンガスの圧力を下げるとメタンハイドレートが分解しやすくなるので、温度を上げるほかに減圧をすることでも、メタンを取り出すことが出来ます。
2) 過飽和状態
通常、メタンや空気などのガスが水に溶ける量は、圧力に比例して大きくなります。高圧で高濃度の状態から圧力を下げると、十分時間が経過した後には平衡状態となり、溶けていた分子の大部分は気体となって抜けてしまいます。しかし、条件によっては、高濃度に溶けた状態が長時間維持されることがあります。馴染み深い例としては炭酸飲料があります。二酸化炭素の水に対する溶解度は高くありませんが、開封後もかなり長い時間溶けたままであることは、日常的に経験することです。
このように、真の安定状態ではないが、大きな乱れが与えられない限り長時間安定に存在できるような状態のことを「準安定状態」といいます。ガスの溶解ではありませんが、水を冷やすと0℃以下でも氷にならず、長時間液体のままとなることがあります。これも準安定状態の代表的な例です。
通常、メタンや空気などのガスが水に溶ける量は、圧力に比例して大きくなります。高圧で高濃度の状態から圧力を下げると、十分時間が経過した後には平衡状態となり、溶けていた分子の大部分は気体となって抜けてしまいます。しかし、条件によっては、高濃度に溶けた状態が長時間維持されることがあります。馴染み深い例としては炭酸飲料があります。二酸化炭素の水に対する溶解度は高くありませんが、開封後もかなり長い時間溶けたままであることは、日常的に経験することです。
このように、真の安定状態ではないが、大きな乱れが与えられない限り長時間安定に存在できるような状態のことを「準安定状態」といいます。ガスの溶解ではありませんが、水を冷やすと0℃以下でも氷にならず、長時間液体のままとなることがあります。これも準安定状態の代表的な例です。
図1
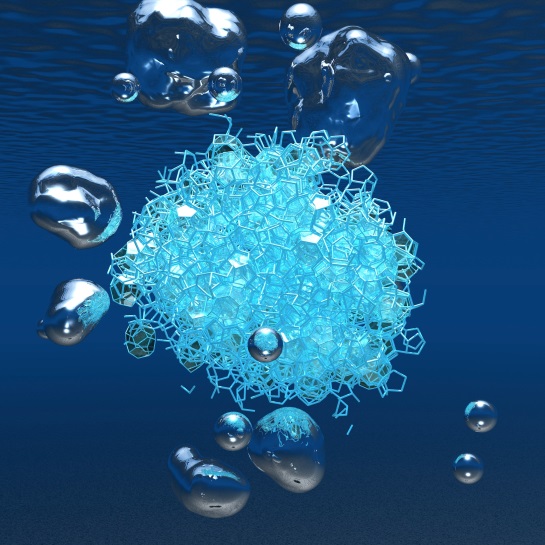
「京」を用いたシミュレーションで得られた、分解途中のメタンハイドレートの様子。中央の水色のかたまりが、分解しつつあるメタンハイドレートの骨格で、分解がある程度進むと、図のようにメタンの気泡が生じ、分解が加速する。融解した水を含めて個々の分子は描いていない。
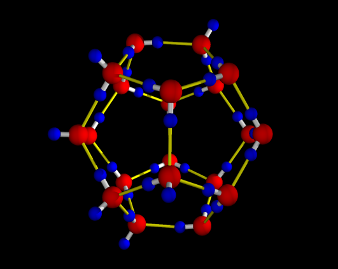
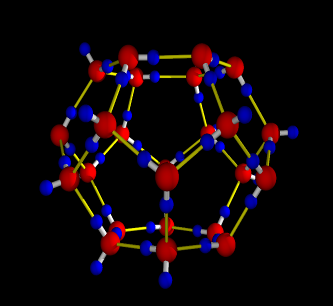
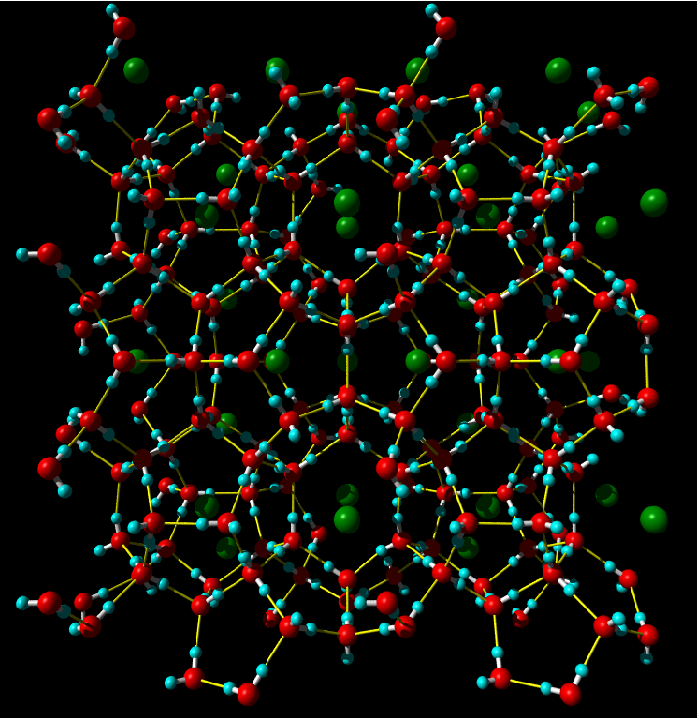
図2
(a)
(b)


(b)

(a) メタンハイドレートを形作る、水分子(赤の酸素と青の水素の球)が水素結合(黄色の線)でで結ばれた12面体と14面体。このカゴ状の多面体の中に、メタン分子が一個づつ入る。
(b) メタンハイドレートの結晶。(a)の多面体が組みあわさって骨格をなし、それぞれにメタン分子(緑の球)が1つずつ入っている。
本研究は、文部科学省HPCI 戦略プログラム(利用課題hp130020、
代表:岡山大学 田中秀樹)及び計算物質科学イニシアティブ(CMSI)
(統括責任者:常行真司 東京大学教授)の助成を受けて行われました。
3) 参考文献
H. Tanaka and M. Matsumoto, Statistical mechanical approach to the thermodynamic stability of clathrate hydrates. Adv. Chem. Phys. 152, 421-462 (2013)
H. Tanaka and M. Matsumoto, Statistical mechanical approach to the thermodynamic stability of clathrate hydrates. Adv. Chem. Phys. 152, 421-462 (2013)
“Methane hydrate dissociation”
(https://www.youtube.com/watch?v=d7Bi_sbrUcs)
発表論文:T. Yagasaki, M. Matsumoto, Y. Andoh, S. Okazaki, and H Tanaka, Effect of Bubble Formation on the Dissociation of Methane Hydrate in Water: A Molecular Dynamics Study. J. Phys. Chem. B 118, 1900 (2013); (DOI: 10.1021/jp412692d.)
報道発表資料はこちらをご覧ください
<お問い合わせ>
岡山大学大学院自然科学研究科(理学部)
理論化学研究室 教授
(氏名)田中 秀樹
(電話番号)086-251-7769
(理論化学研究室のページ)http://theochem.chem.okayama-u.ac.jp